우리 연구실은 규제과학과 임상약과학을 연구합니다.
규제과학은 정부가 기업의 활동 중 국민의 건강이나 안전과 관련된 행위를 조정하는 규제제도의 과학적 토대로, 정부나 산업계가 규제법령을 실질적으로 시행 또는 집행하는 실무분야인 규제업무와는 구별되는 연구의 영역입니다. 자연과학 및 사회과학의 융합과학으로, 의료제품 등을 규제하는 기준치나 조건 등을 어느 정도까지 정해야 안전하고 유용하며 합리적인지에 대하여 연구하는 분야입니다.
임상약과학은 약물치료 임상연구와 실험실연구의 중계역할을 하는 전문연구분야로서 환자의 체내에서 약물의 거동 및 임상적 결과를 탐구하여 새로운 지식을 창출합니다. 개인 간 약물치료 반응의 차이를 규명하기 위해 최신의 연구방법을 활용하며, 약물치료 전문지식을 실험실 또는 통계적 접근법과 연결합니다. 의약품연구에 관한 실험실 기술, 비임상 모델, 임상연구 결과를 통합함으로써 환자의 건강을 증진시키는데 필요한 연구 결과를 제시합니다.
Ph.D. (2001), 임상약과학, 미국 피츠버그대학교 약학대학
Pharm.D. (1996), 임상약학, 미국 미네소타대학교 약학대학
약학석사 (1986), 약품제조화학, 서울대학교 약학대학
약학사 (1984), 제약학과, 서울대학교 약학대학
규제과학/임상약과학 교수 (2015년 9월 – 현재), 서울대학교 약학대학
임상약학/규제과학 교수 (2012년 3월 – 2015년 8월) 연세대학교 약학대학
과학조사관 (2011년 – 2012년) U.S. Food and Drug Administration
임상약리심사관/팀장 (2001년 – 2011년) U.S. Food and Drug Administration
선임연구원/임상팀장 (1986년 – 1992년) 럭키바이오텍연구소
규제입증위원회 위원 (2023년 3월 – 현재) 식품의약품안전처
부회장 (2017년 – 현재) 한국FDC규제과학회
부회장 (2015년 – 현재) 한국임상약학회
중앙약사심의위원회 위원 (2014년 8월 – 현재) 식품의약품안전처
의약품심사 자문위원 (2014년 6월 – 현재) 식품의약품안전평가원
이사 (2014년 – 2022년) 한국희귀질환재단
- 약물노출-반응 관계 (Exposure-Response Relationship) 분석 연구
- 타겟항암제 (Protein Kinase Inhibitors) 연구 및 개발
- 점토광물을 이용한 경구투여 약물의 생물약제학적 특성 개선 연구
- 희귀질환 연구 및 치료제 개발
- 의약품 평가제도 및 개발촉진책 연구
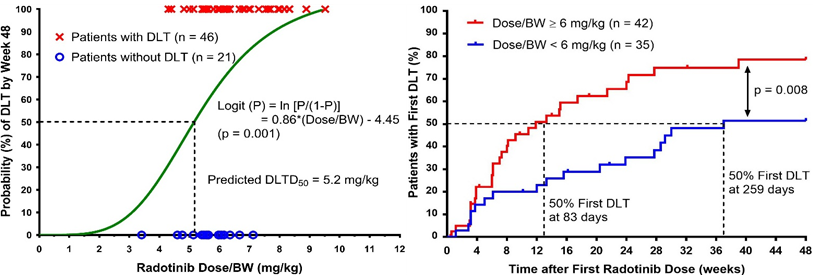
규제과학과 임상약과학이 접목된 연구로서, 만성골수성백혈병 치료제인 라도티닙의 용량 최적화 연구를 예로 들 수 있다. 이 연구에서 환자의 체중당 투여된 라도티닙 용량(Dose/BW)이 증가할수록 용량제한독성 (DLT) 발현이 유의하게 증가한다는 결론을 도출하였다. Dose/BW<6인 환자군과 Dose/BW≥6인 환자군 간의 첫 번째 용량제한독성 발생까지의 시간에 대한 Kaplan-Meier 곡선에 유의한 차이가 있었다. 이를 바탕으로 기존 식약처 허가사항에 따라 모든 환자에게 동일한 용량을 투여하는 것이 아닌, 환자 체중별 맞춤형 용량을 투여할 것을 제안하였다.
- Volumetric absorptive microsampling for the therapeutic drug monitoring of everolimus in patients who have undergone liver transplant. Therapeutic Drug Monitoring. 2023;45(2):223-8.
- Orphan drug designation: a comparison of regulatory systems among United States, European Union, and Republic of Korea. Regulatory Research on Food, Drug & Cosmetic. 2022;2:137-49.
- Appropriate starting dose of dasatinib based on the analyses of dose limiting toxicities and molecular responses in Asian patients with chronic myeloid leukemia. Clinical Lymphoma, Myeloma & Leukemia Research. 2021;21(6):e521-9.
- Development of a limited sampling strategy for the estimation of isoniazid exposure considering N-acetyltransferase 2 genotypes in Korean patients with tuberculosis. Tuberculosis 2021;127:102052.
- Development of a dried blood spot sampling method towards therapeutic monitoring of radotinib in the treatment of chronic myeloid leukaemia. Journal of Clinical Pharmacy and Therapeutics 2020;45(5):1006-1013.
- Population pharmacokinetics of vactosertib, a new new TGF-β receptor type I inhibitor, in patients with advanced solid tumors. Cancer Chemotherapy and Pharmacology 2020;85(1):173-183.
- Pharmacokinetic characteristics of vactosertib, a new activin receptor-like kinase 5 inhibitor, in patients with advanced solid tumors in a first-in-human phase 1 study. Investigational New Drugs 2020;38(3):812-820.
- Comprehensive analyses of safety and efficacy toward individualizing imatinib dosage in patients with chronic myeloid leukemia. International Journal of Hematology 2019;111(3):417-426.
- Association of genetic polymorphisms of CYP2E1, NAT2, GST and SLCO1B1 with the risk of antituberculosis drug-induced liver injury: a systematic review and meta-analysis. BMJ Open 2019;9(8):e027940.
- Determination of a radotinib dosage regimen based on dose-response relationships for the treatment of newly diagnosed patients with chronic myeloid leukemia. Cancer Medicine 2018;7(5):1766-73.
- Antimicrobials for the treatment of drug-resistant Acinetobacter baumannii pneumonia in critically ill patients: a systemic review and Bayesian network meta-analysis. Critical Care 2017;21(1):319.
- Optimization of Radotinib Doses for the Treatment of Chronic Myelogenous Leukemia Based on Dose-Response Relationship Analysis. Leukemias & Lymphomas 2016;57(8):1856-64.